Иммунотерапия при онкологии в москве
Содержание:
- Этот препарат помогает многим пациенткам прожить дольше, но на некоторых HER2-позитивных больных он не действует.
- Новая надежда. Станет ли иммунотерапия панацеей?
- Применение иммунотерапии при разных видах рака
- В России этот метод лечения популярен?
- Иммунотерапия рака: организм сам побеждает опухоль
- Атака клонов. Генетически модифицированный иммунитет
- Как работает иммунная система, и каким образом на неё действует иммунотерапия
- Школа для лимфоцитов
- Препараты для иммунотерапии
- Подготовка к химиотерапии
Этот препарат помогает многим пациенткам прожить дольше, но на некоторых HER2-позитивных больных он не действует.
Кроме того, он весьма токсичен и вызывает множество побочных эффектов — тошноту, высыпания, диарею, головные боли, боли в суставах и др.
Чтобы испытать новую вакцину от рака, учёным нужны были пациенты, в организмах которых не было сильнодействующего герцептина. Поэтому они набрали 11 пациентов в поздней стадии, поражённых другими типами рака, связанного с HER2, потому что практически все пациентки с раком груди принимают герцептин.
Это были пациенты «в такой поздней стадии, что им не помогло никакое лечение, и врачи прогнозировали дальнейшее развитие опухолей», говорит руководитель исследования доктор Джей Берзофский.
Иммунотерапия с использованием новой вакцины предполагает менее мучительные процедуры. Вакцину вводили пациентам в течение шести месяцев. Первые три раза они получали одну дозу раз в четыре недели, а последние две дозы были введены с промежутком в восемь недель.
Этот метод состоит в экстракции иммунных клеток из пациента, видоизменении их в лабораторных условиях, чтобы сделать белок HER2 «видимым», и повторном введении клеток в организм.
Поскольку в лечении используются собственные клетки организма, оно проще переносится и более точечно воздействует на опухоли.
Новая надежда. Станет ли иммунотерапия панацеей?
Как и у других методов лечения рака, у иммунотерапии есть свои ограничения. Несмотря на то, что в ряде случаев пациенты дают очень хороший ответ на терапию ингибиторами иммунных контрольных точек, в 60% случаев либо развивается приобретенная, либо наблюдается первичная резистентность к анти-PD-1 или анти-CTLA-4 препаратам: опухоль просто не реагирует на лечение или быстро приспосабливается и учится его «обходить».
Кроме PD-1, PD-L1/2, CTLA-4, CD28 и B7 на поверхностях Т-клеток и опухолевых клеток есть масса других ко-рецепторов, действие которых пока не изучено так хорошо, как работа контрольных точек, но они также влияют на иммунный ответ. Одно из направлений работы — влияние на эти ко-рецепторы.
Кроме того, терапия ИИКТ дополняется введением вакцин, цитокинов, бета-блокаторов — и такой подход тоже хорошо работает в ряде случаев.
CAR-T терапия все еще является крайне дорогой и пока еще только переходит в стадию коммерческого использования: ведутся разработки в научных группах Эшхара и Розенберга, других исследователей — каждая из групп создают особые виды CAR-Т с направленным действием против определенного вида рака. Но пока это только исследования, проверки и испытания. Пройдет несколько лет, прежде чем это превратится в отработанный массовый способ лечения — но и тогда нельзя будет давать 100% гарантий.
Но пока ученые проводят исследования, врачи внедряют экспериментальные схемы лечения с использованием тех достижений, что уже есть. И самый заметный эффект дает сочетание иммунотерапии с классическими «тремя столпами» онкологии: лучевой и химиотерапией, хирургией. При комбинировании этих методов всегда получается синергия: вместе они работают эффективнее, чем по очереди.
Если стандартно до сих пор иммунотерапевтические препараты включали в третью, в пятую линию (то есть очередь) терапии, то сейчас врачи движутся к тому, чтобы назначать их сразу, вместе с химиотерапией и терапией таргетными моноклональными антителами: такие пациенты часто показывают более хорошую динамику и в итоге живут дольше.
В России уже зарегистрированы все основные иммунопрепараты. Проблема, правда, что для каждого из них Минздрав отдельно оговаривает показания. То есть в оригинальной инструкции к препарату может быть прописано, например, девять разных видов рака, при котором препарат можно назначать, а у нас в стране он зарегистрирован только для шести из них. И так с каждым препаратом. В итоге, пока около 50% опухолей еще не включены в этот список. Соответственно, в рамках лечения по ОМС врач может выписать эти препараты далеко не всем пациентам.
К тому же врачи бюджетных государственных клиник строго ограничены протоколами лечения. И если в протоколе ингибиторы контрольных точек прописаны только на 3 линии, на 3 месте после двух линий стандартной «химии», то выписать их в первую очередь врач просто не имеет права, даже если считает, что пациенту это поможет.
Ну и частая проблема — отсутствие квалификации. Метод, хоть и успел проявить себя, пока для многих врачей в стране еще новый. Препараты все западные, и доходят до нас с опозданием на 2-3 года. А, учитывая, что активно применяется иммунотерапия всего несколько лет, у многих еще нет опыта работы с ними. Кроме того, использование иммунотерапии требует специфических знаний.
В частной медицине мы не ограничены бюджетом. Если в «Медицину 24/7» обращается пациент с такой опухолью, для которой еще не зарегистрирован препарат иммунотерапии, мы предлагаем ему пройти молекулярно-генетическое исследование. По результатам становится понятно, отреагирует ли его опухоль на иммунопрепарат. Если да — врач имеет полное право ее назначить. Поэтому в нашем стационаре мы применяем иммунотерапию почти по всем видам рака — она дает очень хорошие результаты. Даже пациенты на III-IV стадии показывают улучшения. Иммунопрепараты дают нам возможность продлять людям жизнь, даже в случаях, которые считались безнадежными.
Общее и в частных, и в государственных клиниках — это сами пациенты. Они не всегда хорошо понимают, что это за метод, как он работает, отсюда недоверие. Мы надеемся, эта статья помогла разобраться и понять, что иммунотерапия сегодня совершенно заслуженно находится в фокусе пристального внимания онкологов. Судя по результатам, она уже готова встать на один уровень с классическими методами. Страшная болезнь отступит еще на шаг дальше.
Применение иммунотерапии при разных видах рака
Биотерапия не зря считается действенным методом в борьбе с онкологическими поражениями. Как показывает клиническая практика, собственные силы организма способны уничтожать аномальные структуры, локализованные в совершенно разных органах.
На сегодняшний день у онкологов есть безопасное биологическое лекарство от следующих разновидностей злокачественных новообразований:
- Иммунотерапия при раке почки, выявляемом обычно на самых последних стадиях и практически никогда не реагирующем на облучение и химию, позволяет значительно усилить воздействие собственного иммунитета больного, что приводит к разрушению иммунной системой атипичных клеток и приостановке роста онкоопухоли.
- При раке матки клеточная иммунотерапия, направленная на уничтожение злокачественной структуры, применяется чаще всего на 3 или 4 стадии, когда общепринятые методы лечения перестают действовать. Назначение иммунотерапии на этом этапе позволяет продлить жизнь женщины на максимально длительный срок и сохранить её качество.
- Иммунотерапия при раке мочевого пузыря, одной из самых тяжёлых и опасных патологий, также показывает высокую эффективность. Не так давно для такого лечения применялась только вакцина БЦЖ, которую вливали пациенту внутрипузырно. В 2018 г. в России появился новый препарат для разрушения этой разновидности опухолевой структуры – Тецентрик, который стал первым ингибитором PD-L1. С его помощью качество лечения раковых структур уротелиального типа повысилось в несколько раз. Этим же препаратом проводится и иммунотерапия при раке легких, немелкоклеточной его форме, которая также плохо поддаётся химиотерапии.
Высокую эффективность биотерапия показывает и в лечении рака желудка, при раке поджелудочной железы и раке печени. Этот метод позволяет не только разрушать мутировавшие клетки в перечисленных органах, но и уничтожать вторичные злокачественные очаги. А вот при раке кишечника иммунотерапия недостаточно результативна. Как показывает практика онкологов, на сегодняшний день основная часть злокачественных новообразований этого органа невосприимчива к такому виду терапии. По мнению специалистов, иммунная система просто «не видит» эту разновидность опухоли, но исследования продолжаются и, возможно, в скором времени будут найдены вакцины от раковых опухолей кишечника.
В России этот метод лечения популярен?
Нет. Некоторые препараты, например пембролизумаб, ниволумаб, ипилимумаб и атезолизумаб, зарегистрированы в России. Но о широком доступе к терапии говорить не приходится. Препараты зарегистрированы не по всем показаниям, и во многих ситуациях назначить их можно только офлейбл (не по инструкции), но тогда лечение нельзя будет получить бесплатно по полису ОМС.
Кроме того, курс лечения, по словам Петра Сергеева, может стоить от 180 000 до 800 000 рублей в месяц. «В себестоимость заложены миллионы долларов, потраченных на исследования, а дешевых аналогов (дженериков) в иммунотерапии пока не существует, — объясняет врач. — Частная клиника нашего уровня может закупить все препараты и проконтролировать их оригинальность, чтобы в нашей аптеке они были доступны пациентам в любой момент. Но мы не можем сделать цену ниже, чем у производителя. Со временем, когда этот метод лечения станет более массовым, препараты должны подешеветь и стать более доступными. Такой путь проходят многие лекарства. В первые годы после войны производство пенициллина было недостаточным, он был дорог, но уже в 1952 году стал производиться по улучшенной технологии и сильно подешевел».
Сегодня в России получить иммунотерапевтические препараты иногда позволяет так называемая региональная льгота, которая регулируется законом о социальной помощи, но такие закупки финансируются бюджетом только в некоторых регионах. Кроме того, можно попытаться попасть в программу клинических исследований, такая возможность есть и в клинике «Медицина 24/7», или же выбрать платное лечение в медицинском учреждении, где уже применяют иммунотерапию.
Иммунотерапия рака: организм сам побеждает опухоль
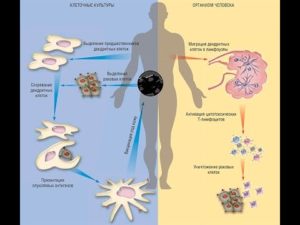
Иммунотерапия — новый способ борьбы с онкологией. Методика направлена на то, чтобы иммунитет самостоятельно боролся со злокачественными клетками.
Иммунная система человека призвана защищать организм от болезнетворных микроорганизмов и переродившихся патологических клеток. Если защитные клетки ослабевают, может развиться рак.
Почему возникает онкозаболевание?
- Патологическая клетка вырабатывает мало чужеродного вещества, поэтому иммунная система ее не замечает.
- Новообразование вырабатывает вещества, которые подавляют работу иммунной системы.
Препараты иммунотерапии активизируют защитные силы организма для борьбы с опухолью.
Виды препаратов иммунотерапии
- Моноклональные антитела. Первый вид прикрепляется к раковым клеткам — так иммунная система сможет распознать и уничтожить опухоль. Другой вид моноклональных антител способствует тому, чтобы препараты химиотерапии попадали именно в клетки опухоли и не действовали на здоровые ткани.
- Ингибиторы контрольных точек. Контрольные точки необходимы, чтобы защитные клетки организма не атаковали нормальные клетки. Опухоль использует их, чтобы “обмануть” иммунную систему. Ингибиторы угнетают действие контрольных точек, и защитные клетки уничтожают опухоль.
- Модуляторы. Активизируют иммунную систему в целом.
- Вакцины против онкозаболеваний. Ученые установили, что рак шейки матки вызван папилломавирусом человека. Против этой инфекции можно сделать прививку.
При лечении онкологических заболеваний чаще других применяют моноклональные антитела.
Показания для иммунотерапии
Врачи назначают препараты иммунотерапии при онкологии на разных стадиях заболевания. Если опухоль поразила только один орган и нет метастазов, иммунопрепараты помогут добиться стойкой ремиссии. На поздних этапах они уменьшают размеры опухоли и повышают шансы на выздоровление.
Преимущества и недостатки иммунотерапии
Ценность препаратов иммунотерапии в том, что они помогают пациентам в тех случаях, когда другие методы и препараты недостаточно эффективны. Иммунопрепараты усиливают действие химиотерапии, так как переносят действующие вещества непосредственно в опухоль. Терапия стимулирует защитную систему организма, поэтому снижается риск рецидива.
Главный минус иммунотерапии в том, что пока лекарства существуют не против всех возможных видов заболевания.
Те же, которые доказали свою эффективность, действуют только на опухолевые клетки. Поэтому побочные эффекты во время их приема развиваются реже, чем при химио- или радиотерапии, но все же они возможны.
Побочные эффекты при иммунотерапии
Препараты иммунотерапии не являются токсичными. Наиболее частые нежелательные последствия во время лечения:
- слабость;
- тошнота;
- покраснение кожи.
Иммунная система каждого человека индивидуальна, и в редких случаях защитные клетки организма атакуют здоровые ткани. Поэтому лекарства данной группы принимают под контролем врача. Он следит за малейшими изменениями в состоянии пациента и, при необходимости, вовремя корректирует лечение.
Кейтруда эффективнее химиотерапии
Меланома — это агрессивная разновидность рака кожи. Клетки, которые вырабатывают меланин, перерождаются в злокачественные. Заболевание протекает стремительно, в течение короткого периода времени появляются вторичные очаги опухоли — метастазы. Они могут привести к отказу жизненно важных органов.
При лечении меланомы на поздних стадиях доктора применяют иммунотерапевтические препараты Кейтруда (пембролизумаб), Опдиво (ипилимумаб) и Ервой (ниволумаб).
Исследования доказали, что лекарство Кейтруда в полтора раза эффективнее, чем химиотерапия. В группе пациентов, которые принимали это лекарство, опухоли уменьшились у каждого второго пациента. После химиотерапии злокачественные образования уменьшились у каждого третьего.
Лекарство позволяет иммунной системе выявлять раковые клетки. В состав препарата входят вещества, которые “выключают” белок PD-1. Он не дает защитным клеткам распознавать опухоль.
Иммунотерапия и рак груди
Препарат Кейтруда используют и для лечения рака молочной железы.
Показания для применения:
- В клетках опухоли есть мутация гена BRAF.
- Опухоль невозможно удалить хирургическим путем, а другие методы лечения не действуют.
Лекарство и его дозировку выбирает врач в зависимости от стадии болезни и состояния пациента.
Атака клонов. Генетически модифицированный иммунитет
Ингибиторы иммунных контрольных точек заслуженно находятся в центре внимания, но этот механизм пока небезупречен и не может вылечить любой рак. Хорошо, что в иммунотерапии активно развиваются смежные направления исследований. Одно из самых многообещающих — CAR-T терапия.
Буква Т в названии метода — все те же неизменные Т-клетки нашего иммунитета. CAR (Chimeric antigen receptor) — это химерный рецептор антигена. Почему рецептор называют химерным? Потому что он собран из нескольких частей, взятых от разных клеток — с помощью умений генных инженеров.
У обычной Т-клетки есть особый рецептор TCR (T-cell receptor). Он «ощупывает» все клетки организма на своем пути и, если чувствует на поверхности клетки какую-то чужеродную молекулу, посылает Т-клетке активирующий сигнал. Та, в свою очередь, либо расправляется с нежелательным пришельцем сама, либо выделяет специальные активные вещества (цитокины) и призывает другие клетки иммунитета «разобраться». Убивают Т-клетки весьма эффективно.
Правда, не очень точно. Разновидностей TCR у нас куда меньше, чем существует антигенов. Поэтому Т-клетки умеют распознавать своим TCR много антигенов, но — только приблизительно. Раковые клетки часто пользуются этой слабостью нашей системы безопасности и притворяются «своими».
Эволюция решила проблему как умела: в организме человека есть еще один механизм выявления чужаков: антитела. Это особые белки, которые выделяются другим классом иммунных клеток: B-лимфоцитами. У В-клеток, в отличие от Т-клеток, к каждому «клиенту» индивидуальный подход.
Антитело представляет собой белковую структуру в виде буквы Y. На обоих концах этой «вилки» есть участки, связывающиеся с антигеном. Эти участки могут изменяться у каждого следующего поколения антител, чтобы плотнее прилегать к антигену — как подбор кусочков паззла. При обнаружении чужеродного антигена В-клетки выделяют миллиарды антител, среди которых идет отбор на самое точное соответствие антигену. В итоге получаются эталонные антитела, «натасканные» специально для очень точного распознавания конкретного «чужака» — антигена.

Антитело, приспособленное находить определенный антиген
Однако, распознать — не всегда означает обезвредить. С этим у антител сложности — самостоятельно уничтожить «врага» они могут далеко не во всех случаях.
Так вот, в 1989 году израильский химик и иммунолог Зелиг Эшхар придумал объединить убийственную мощь подслеповатых Т-клеток и снайперское прицеливание антител. Он выделил концевые участки белков-антител, которые способны плотно связываться с антигеном определенных раковых клеток, и «пересадил» их в Т-клетку — заменил ими часть TCR, отвечающие за распознавание антигенов.
Впоследствии он начал работать совместно с американским коллегой, Стивеном Розенбергом, у них получилось сделать химерный рецептор более эффективной конструкции, одновременно чувствительный и избирательный.

Разница между обычными Т-клетками и CAR-T-клетками
Исследования в пробирке показали хороший результат. Затем ученые снова лечили мышей, затем кропотливо переносили методику на человека.
Со временем терапию CAR-T привели к современному виду.
- Сначала с помощью генно-молекулярного тестирования определяют специфические мутации в опухолевых клетках человека, на которые можно «настроить» антитела.
- Затем у человека берут его собственные Т-клетки, изменяют с помощью биоинженерных методов, вместо TCR «пересаживая» CAR, настроенный на выявленные мутации.
- Затем модифицированные CAR-T клетки размножаются в пробирке и вводятся обратно в организм человека, где они успешно распознают и убивают раковые клетки.
В клинических исследованиях, начатых в 2010 году, сразу получились обнадеживающие результаты: в лечении лимфомы 12 из 13 пациентов показали улучшение, а у 4-х наступила ремиссия. При лечении лейкемии ремиссия наступила у 17 человек из 33.
В 2018 в Nature Medicine появилась статья американских онкологов, где сообщалось, что уже два года они наблюдают пациентку, полностью здоровую после CAR-T терапии. Ее вылечили от метастатического рака молочной железы с метастазами. Это ее фотография в каяке приведена в начале статьи: после лечения она вернулась на работу и ходит в походы.
Как работает иммунная система, и каким образом на неё действует иммунотерапия
Иммунная система человека неоднородна. Нельзя воспринимать её как одного «стража», который обеспечивает защиту организма от чего угодно. Это большое «войско», целая система различных молекул и клеток, которые взаимодействуют между собой. Одна их часть активна, вторая находится в состоянии покоя, третья – в стадии активации. Какая-то группа этих клеток чем-то подавлена, какая-то – вырабатывает то, что борется с патологическими процессами или, наоборот, то, что их запускает.
По функциям их можно условно разделить, например, на «солдат», которые обеспечивают защиту; «спецназ», выполняющий особые задания; «полицейских», которые все контролируют; «учителей», ответственных за обучение и др. Этот список можно продолжить, так как иммунные клетки играют много различных ролей.
Иммунитет – особая биологическая система в пределах нашего организма, которая работает по своим сложным алгоритмам. Она обладает способностью активироваться при любом инфекционном, воспалительном процессе, в то же время у неё есть и собственные подавляющие механизмы.
Когда опухолевые клетки только зарождаются в организме человека в результате генетических мутаций, влияния канцерогенных факторов и др., иммунная система их уничтожает. Но на каком-то этапе вдруг наступает сбой, и происходит её торможение. На самом деле, это нормальная, непатологическая функция иммунитета, которая включается и у здорового человека.

В чём её назначение? Известен целый ряд аутоиммунных (ревматических) заболеваний, при которых иммунная система начинает вырабатывать антитела и бороться с собственными клетками. Это происходит при системной волчанке, ревматоидных артритах и ряде других заболеваний. У пациентов с такими диагнозами здоровые суставы и мышцы поражаются собственной иммунной системой. В организме здоровых людей этому препятствуют специальные механизмы торможения/блокировки. Развиваясь, злокачественный процесс их запускает, и они блокируют иммунный ответ. Опухоль набирает силу. Наступает процесс равновесия, когда иммунная система ещё контролирует патологические клетки, но справляется с ними уже с трудом. Потом происходит ускользание, иммунная система перестаёт распознавать опухоль, которая начинает бесконтрольно расти и распространяться по всему организму.
Однако, страдает только противоопухолевый иммунитет, а все остальные виды иммунитета, например, противоинфекционный, работают. Можно сказать, что «обыденный» иммунитет, продолжает стоять на страже здоровья онкологического пациента и защищать его, например, от вирусов.
Необходимо очень тонко воздействовать на противоопухолевый иммунитет с помощью современных имунноонкологических препаратов, чтобы снять все возникшие факторы торможения.

Цель иммунотерапии – помочь собственной иммунной системе бороться с опухолью. Это единственное направление современной лекарственной терапии, которое не предполагает введения ядовитых веществ – молекул, которые влияют на биологию опухоли. Иммунотерапия разблокирует собственную иммунную систему человека, заставляет её снова активно уничтожать патологические клетки. Ведь работают не чужеродные лекарственные препараты, а собственная иммунная система пациента.
Школа для лимфоцитов
Взаимодействие иммунной системы и опухоли проходит три этапа:
- элиминация. Заключается в эффективном распознавании чужих клеток. Известно, что раковые клетки могут периодически возникать у всех людей, но хорошо функционирующая иммунная система может их обнаружить и уничтожить. Однако иногда злокачественные клетки ускользают от разрушения и болезнь переходит в следующую стадию.
- «спящий» рак. Те клетки опухоли, которые смогли избежать уничтожения, начинают усиленно размножаться.
- прогрессия опухоли происходит за счёт усиленного деления злых клеток, способных подавлять иммунную систему или уклоняться от её воздействия, новообразование продолжает захватывать организм.
Иммунотерапии рака связана с открытием так называемых контрольных точек иммунитета, которые не позволяют нашей защитной системе проявлять свою противоопухолевую активность. Именно эти точки и защищают опухоль, делая её невидимой для иммунитета. Соответственно, заблокировав их с помощью инновационных препаратов, можно перезапустить иммунную систему, добившись от неё формирования адекватного противоопухолевого ответа. В результате переученные Т‑лимфоциты уже могут распознавать, атаковать и уничтожать чужеродные раковые клетки. При этом таких побочных эффектов, как при химиотерапии, при иммунотерапии не возникает и госпитализация не требуется – всё делается амбулаторно.
Препараты для иммунотерапии
Большинство применяемых для этих целей препаратов является либо иммунодепрессантами, либо иммуностимуляторами. В иммунодепрессивной терапии применяют как биол, препараты (напр., антилимфоцитарная сыворотка — АЛС, содержащая антитела, направленные против лимфоцитов), так и хим. синтетические соединения (имуран, циклофосфан, цитозин-арабинозид и др.). Стимуляторы иммунитета также бывают биологическими (напр., вакцина БЦЖ) и химическими (напр., левомизол). Для заместительной и адоптивной терапии применяют биол, препараты — иммунокомпетентные клетки и их компоненты.
Подготовка к химиотерапии
Применение таргетной и иммунотерапии не требует соблюдения особого режима или диеты — рекомендуются достаточный сон, регулярное здоровое питание, иногда прием поливитаминов.
При проведении химиотерапии затрагиваются и здоровые клетки, нужен «строительный материал» для восполнения потерь белка. Поэтому в рацион активно должны включаться бобовые, нежирные мясо и рыба, птица. Также целесообразен дополнительный прием витаминов группы В. Полезны любые виды сырых и отварных овощей, салатов и фруктов, а особенно с повышенным содержанием витамина С- цитрусовые, яблоки, смородина. Также желательно увеличить количество жидкости, употребляя овощные, фруктовые и ягодные соки. Целесообразность этого значительно возрастает при лечении препаратами платины. Особенно полезны морковный, свекольный, томатный, малиновый и брусничный соки.